
取消
清空記錄
歷史記錄
清空記錄
歷史記錄







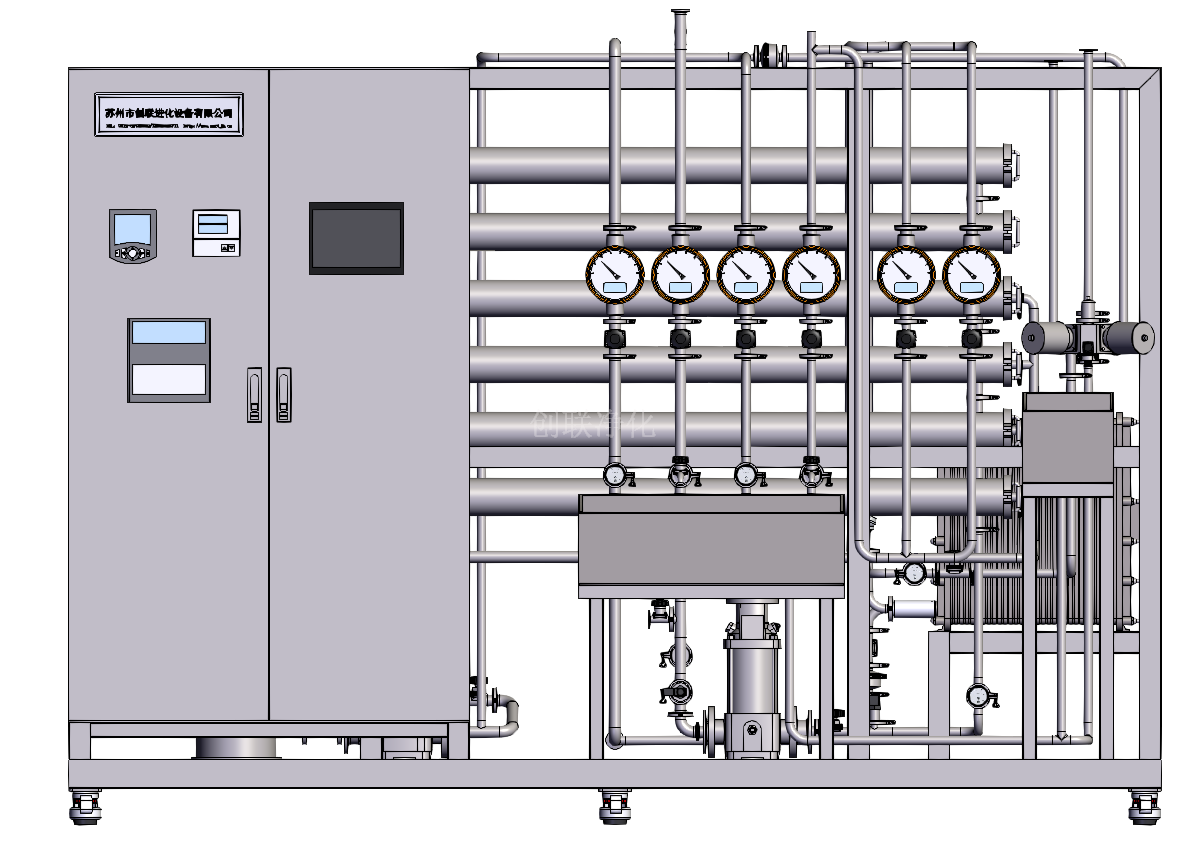
制藥行業純化水設備及注射水設備
制藥純化水設備用途:
藥品原料、中間產品提純用純化水設備
生物制藥、化學制藥用純化水設備
獸藥生產用純化水設備
保健品、口服液、保健酒、功能飲料生產用純化水
化妝品生產用純化水設備
注射用水的原水
中藥生產提純用純化水
其它制藥工藝用水
設計參考標準
中國藥典GMP2025版純化水標準
歐盟和FDAG MP規范和實施指南
藥用純化水制備裝置JB/T20194-2019
醫藥工藝用水系統設計規范GB50913-2013
一般處理工藝:
預處理+二級反滲透+儲存分配系統工藝
預處理+二級反滲透+EDI+儲存分配系統工藝
根據滅菌方式不同,一般分為預處理+儲存分配系統巴氏滅菌和預處理、反滲透、EDI和儲存和分配系統全程巴氏滅菌工藝。
純化水設備技術要求:
● 執行中國藥典GMP和FDA純化水要求;
● 實現工藝全過程熱消毒,對微生物控制更好;
● 單體設備滿足GMP要求,材料選擇優先選擇316L(預處理304);
● 設備實現全自動運行,自動清洗、運行、一鍵滅菌,審計追蹤功能。
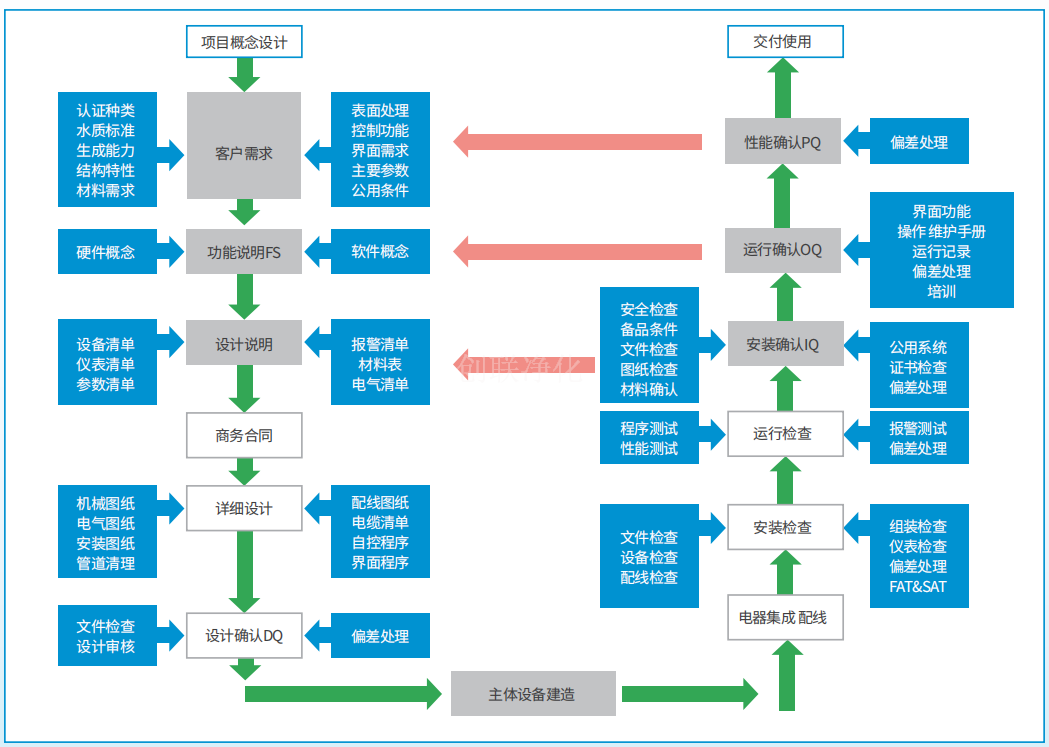
● 提供設備所需要的DQ\FAT\SAT\IQ\OQ\PQ文件支持。
● 系統停機狀態下實現自動微循環,防止死水,降低微生物污染風險。
施工規范和選材(參考GMP規范、藥用純化水制備裝置、醫藥工藝用水系統設計規范)
■按照中國GMP要求及FDA技術要求,優先選擇衛生級不銹鋼316L/304材料
■按照藥用純化水制備裝置標準選擇粗糙度≤0.63μm,工藝接觸部分選擇粗糙度≤0.4μm.
■管道保持有0.5~2%(5mm/m~20mm/m)的安裝坡度;
■工藝用水帶支管閥門管路安裝死角≤3D標準
■循環管道回水流速不小于1.0m/s,循環回水流量大于泵的出口流量的50%。
■單管循環輸送總長度小于400m,管道直徑不超過DN65(如果實際長度高于此指標,采用多路供水方式)。
■焊接氬氣標準應不低于99.999%

焊接目視標準一般不得高于3級標準
創聯凈化技術團隊配合客戶完成相關驗證工作,包括但不限于URS/DQ/FAT/SAT/IQ/OQ/PQ文件,真正實現交鑰匙工程,減少客戶不必要的工作。
實力創聯凈化
成立于2005年的蘇州市創聯凈化設備有限公司,目前是國家高新技術企業,省級專精特新企業,目前已經為國內外上千家客戶提供了設備及服務,提供整機2年的長時間質量保證。


 瀏覽器自帶分享功能也很好用哦~
瀏覽器自帶分享功能也很好用哦~





